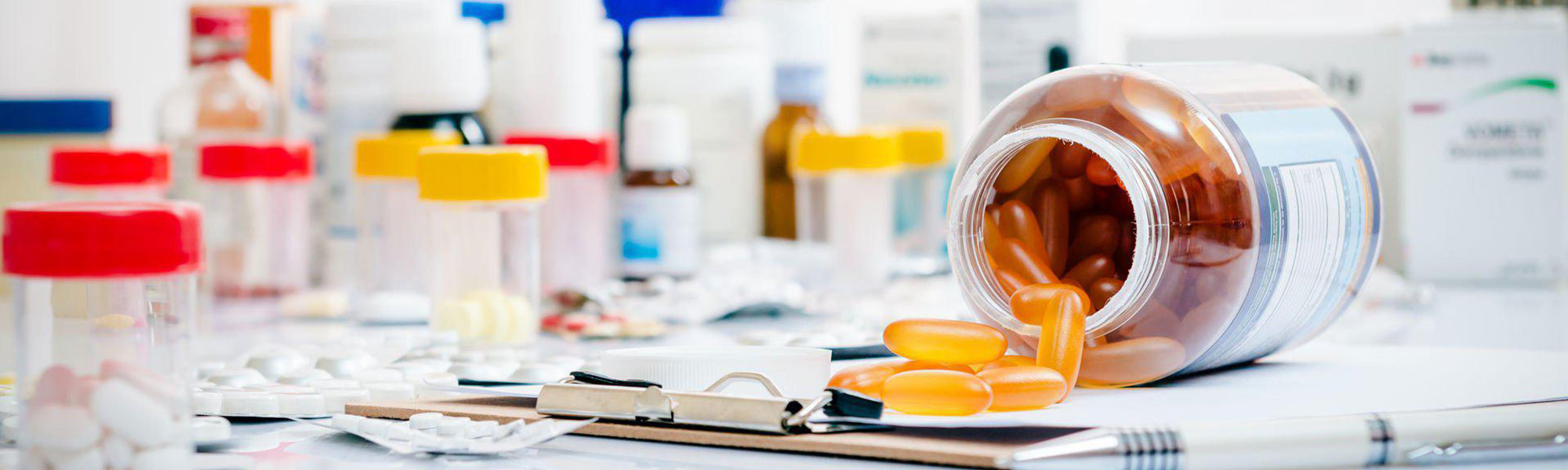
Правила GLP применяют в отечественных лабораториях, работающих на фармацевтическом рынке, и они напрямую связаны с безопасностью лекарственных средств.
Безопасность и эффективность – ключевые цели при разработке лекарств. Этот процесс немыслим без исследования препаратов и компонентов, которые в будущем могут войти в состав медикаментов. В своей работе разработчики лекарств применяют признанные во всем мире правила GLP – как залога безопасности конечного продукта для здоровья человека и экологии. Что такое GLP-исследования, как они связаны с качеством лекарств и почему эти знания важны для среднестатистического покупателя?
Что такое GLP и почему это важно?
В переводе с английского GLP или «Good Laboratory Practice» означает «Надлежащая лабораторная практика». GLP — это целая система норм и правил, регулирующая организационный процесс и условия, при которых проводят исследования лекарств в лабораторных условиях.
Целью таких исследований является получение данных о безопасности лекарственных средств, а также веществ, которые содержатся в лекарственных препаратах. Главная задача GLP – обеспечить возможность полного прослеживания всего хода исследования и доказательства правильности его проведения.
GLP-принципы в Казахстане: особые лаборатории
Принципы надлежащей лабораторной практики (на примере токсикологических лабораторий) применяют и в Казахстане. В частности, в Алматы на базе лаборатории фармакологических испытаний территориального филиала Национального центра экспертизы лекарственных средств и медицинских изделий Министерства здравоохранения РК. Исследования здесь проводятся по двум направлениям. Одно из них – фармакокинетические испытания. Речь идет о разделе фармакологии, который изучает закономерности химических и биологических процессов, происходящих с лекарственным средством в организме человека или животного. Второе и так же очень важное направление – доклинические исследования in vitro и in vivo. Это – экспериментальные исследования влияния лекарственных препаратов на организм животных (in vivo) или на моделях клеток (in vitrо) до того, как они поступят на фармацевтический рынок (в аптеки). Их цель – установить безопасность и эффективность фармакологических веществ, лекарственных препаратов и выявить вероятность возникновения побочных эффектов.
Персональные требования к сотрудникам. Зачем это?
Для получения статуса GLP-лаборатории любой направленности есть ряд высоких требований. В первую очередь, к персоналу. В алматинском филиале лаборатории Национального центра экспертизы лекарственных средств работают обученные и профессиональные сотрудники, понимающие методологию проведения экспериментов и умеющие делать верные заключения и выводы. Это специалисты с медицинским, биологическим и химическим образованием. Весь персонал подготовлен в соответствии с требованиями и концепцией GLP. Один из важнейших принципов GLP – обеспечение надлежащей системы документирования. Что не записано – то не проведено. Это требование или принцип любой качественной практики. И лаборатория строго придерживается этого правила. Каждый этап фиксируется записями от момента поступления лекарственного препарата в лабораторию до итогового отчета. Важное требование GLP-лабораторий – отлаженная система обеспечения качества во главе с ответственным независимым лицом. По правилам он не участвует в проведении экспериментов. Постоянный контроль за исследованиями в лаборатории осуществляет ответственное лицо – уполномоченный по качеству. Следуя утвержденному плану проверок, он как цербер, строго контролирует все действия и фиксирует их в документах. В GLP-лаборатории ТФ г. Алматы создан такой отдел качества. Его сотрудники проходят соответствующее обучение и имеют опыт, необходимый для исполнения своих обязанностей.
«Грязные» и «чистые» зоны лабораторий
Другой немаловажный принцип GLP – соответствующие условия и требования к помещениям и оборудованию, а также особый порядок снабжения и хранения основных и вспомогательных материалов. Имеющееся лабораторное испытательное оборудование проходит метрологический контроль по утвержденному плану поверок. Все это подтверждается маркировкой на оборудовании и сертификатами соответствия.
Если экспериментальные работы предполагают in vivo исследования (то есть эксперименты на живом организме) на животных, особую актуальность приобретают требования к виварию и содержанию лабораторных животных. В таком случае выделяются «чистые» и «грязные» зоны для исключения контаминации – попадании посторонних микроорганизмов в биологический образец или культуру.
Немаловажное требование к лабораториям, планирующим проведение GLP-аккредитации – соответствие помещений и оборудования установленным стандартам. Помещения должны быть разделены на зоны с ведением записей по климат-контролю. В лабораториях есть строго контролируемые зоны с ограниченным в них доступом, к примеру, для хранения стандартных и испытуемых образцов. Такие же правила ограниченного доступа действуют для архива лаборатории.
В соответствии с требованиями GLP большая ответственность ложится на руководителя исследования. Он является главным контролирующим лицом в исследовании, несет ответственность за общее проведение испытаний исследования и подготовку заключительного отчета.
Отдельно следует выделить ведение документации. Она должна быть прослеживаемой с подтверждением записями на каждом этапе исследования. Для этого в лаборатории должны быть разработаны и утверждены стандартные операционные процедуры (СОПы), листы учета материалов, формы ведения записей.
Согласно требованиями GLP, в лаборатории должна быть внедрена валидация компьютеризированных систем и расчетных систем и программ. Это сложный процесс, требующий обучения сотрудников знаниям по оформлению и ведению документов, огромный и кропотливый труд. Однако при выполнении всех условий успех лаборатории в прохождении аккредитации будет обеспечен.
Что дает GLP-аккредитация?
Аккредитация любой лаборатории означает знак качества. Это дает официальное признание независимым органом по аккредитации того, что лаборатория действует согласно международным требованиям и правилам. Сертификат аккредитации прежде всего дает взаимное признание результатов испытаний. Кроме того, сертифицированная лаборатория имеет опыт и знания, а значит и доверие к таким лабораториям больше.
Лаборатория НЦЭЛС имеет международный сертификат GLP OECD, выданный SNAS Словацкой национальной аккредитационной службой в 2018 году. В текущем году пройдена очередная инспекция с выдачей сертификата до 2023 года. Вся документация оформляется в соответствии с установленными требованиями и процедурами GLP. Планируется расширение области аккредитации в будущем году.
Правила GLP: спектр применения широкий
Правила надлежащей лабораторной практики применяют не только в неклинических исследованиях по безопасности испытуемых веществ, которые содержатся в лекарственных средствах, но также и в пестицидах, косметических средствах, ветеринарных препаратах. Правила GLP используют в проведении исследований пищевых и кормовых добавок, промышленных химических веществ, медицинских изделий.
Стандарты GLP в мировой практике
Система GLP действует больше 20 лет. Одними из первых стандарты GLP разработали в США применительно к разработкам, использующим токсические вещества. Сначала их сделали обязательными для всех производств Соединенных Штатов, позже – в отношении химических и фармацевтических производств других государств, экспортирующих продукцию в эту страну.
После этого правила GLP распространились на страны, входящие в Организацию экономического сотрудничества и развития и получили широкое распространение в мире. В некоторых европейских государствах стандарт GLP является обязательным при разработке любых новых видов химической продукции.
Справочно. С 2018 года Лаборатория фармакологических испытаний (г. Алматы) сертифицирована на соответствие требованиям GLP OECD («Надлежащая лабораторная практика» Организации экономического сотрудничества и развития) Словацкой национальной аккредитующей службой (SNAS).
Все испытательные лаборатории предприятия – испытательный центр с лабораториями территориального филиала в городе Алматы, испытательные лаборатории отделений в городах Караганда и Тараз – аккредитованы в системе технического регулирования на соответствие требованиям стандарта ISO/IEC 17025.
В свою очередь, ISO/IEC 17025 позволяет лабораториям продемонстрировать то, что они компетентно выполняют работу и предоставляют достоверные результаты, тем самым повышая уровень доверия к своей работе, как на национальном, так и глобальном уровнях.